An ultrafast rechargeable aluminium-ion battery
Nature, 520, 324–328 (2015)
DOI: 10.1038/nature14340
Meng-Chang Lin1,2*, Ming Gong1*, Bingan Lu1,3*, Yingpeng Wu1*, Di-Yan Wang1,4,5, Mingyun Guan1, Michael Angell1, Changxin Chen1, Jiang Yang1, Bing-Joe Hwang6 & Hongjie Dai1
1 Department of Chemistry, Stanford University, Stanford, California 94305, USA.
2 Green Energy and Environment Research Laboratories, Industrial Technology Research Institute, Hsinchu 31040, Taiwan.
3 School of Physics and Electronics, Hunan University, Changsha 410082, China.
4 Department of Chemistry, National Taiwan Normal University, Taipei 11677, Taiwan.
5 Institute of Atomic and MolecularSciences, Academia Sinica, Taipei 10617, Taiwan.
6 Department of Chemical Engineering, National Taiwan University of Science and Technology, Taipei 10607, Taiwan
-----------------------------------------------------------------------------------
この論文はオープンアクセスになってはいないが,Researchgate関連の以下のURLでダウンロードできる。
https://www.researchgate.net/publication/274643288_An_ultrafast_rechargeable_aluminium-ion_battery
以下では,上記のURLで表示されるpdfファイルのページ番号やFig等を示して説明する(著作権のため)。
---------------------------------はじめに---------------------------------------
この論文が,高速充電可能なアルミニウムイオン二次電池に関する先駆けとなっている。
(アルミニウム二次電池【1】:超高速充電可能なアルミニウムイオンバッテリ ーにおける
GMG社のグラフェンーアルミニウムグラフェンーアルミニウムイオンバッテリー記事の性能データ表の参考文献2)
アルミニウム二次電池【1】での,GMGのグラフェンーアルミニウムイオンバッテリーとの違いは,
カソード電極用のカーボン材料が,GMGではグラフェンであるのに対して,
この論文で用いられているのは,以下のような,グラファイト系のカーボン材料である点となっている。
そのため,論文中では,”Rechargeable Al/graphite cell”とされている。
The cathode was made from either pyrolytic graphite (PG) foil (~17 μm) or a three-dimensional graphitic foam.
まず,どのような材料を用いて,どのような条件で実験が行われたのかを実験項から見ていくこととする。
(実際の実験の細部を把握できないままに,数値等の結果のみを見てしまうと,重要な点を見誤ることもあるため。)
-------------------------------------------------------------
METHODS
(カソード電極材料)
実験で使われたカーボン材料は,以下の3種で,いずれもグラファイト系のカーボンとなる。
Natural graphite, PG(pyrolytic graphite)foil and graphitic foam
Natural graphite foil 天然黒鉛箔
天然黒鉛箔は、膨張黒鉛フレ ー クを圧縮することによって製造され、天然黒鉛フレ ー ク間のファンデルワ ー ルス結合によって積層が起こる。
(天然黒鉛箔は充放電で顕著な体膨張が起こってしまうのに対して,分解黒鉛箔では体膨張が起こらないことが,Extended Data Figure 8の写真で示されている。しかし,容量的には,天然黒鉛箔が最も高いものであった。←層間が一番スカスカなので?)
Pyrolytic graphite (PG) foil 熱分解黒鉛箔
PG 箔はボリイミドを高温で熱分解することにより合成されており、欠陥により必然的に共有結合が生成される。
PG foil (0.017 mm, Suzhou Dasen Electronics Materials)とされているので,PG箔としては市販品が用いられている。
Graphitic foam グラファイトフォーム(グラファイト発泡体。その形状に関しては,Fig.2a参照)
ニッケルフォーム (Alantum Advanced Technology Materials, Shenyang, China)を,グラファイトフォ ー ムのメタンガスを用いたCVD 成長用の 3D 足場テンプレ ー トとして用いて調製している。
(アノード電極材料)
Aluminium foil アルミニウム箔(thickness,15–250 μm)
(電解質)
イオン液体([EMIm]Clと塩化アルミニウムAlCl3とを脱水処理した後に,アルゴン気流下グローブボックス中で混合することで調整している。(The water content of the ionic liquid was determined 500–700 p.p.m.)
イオン液体([EMIm]Clと塩化アルミニウムAlCl3とのモル比は,1.1~1.8
A room temperature ionic liquid electrolyte was made by mixing 1-ethyl-3-methylimidazolium chloride ([EMIm]Cl, 97%,
Acros Chemicals) and anhydrous aluminium chloride (AlCl3, 99.999%, SigmaAldrich).
(バッテリーのスケールアップにおいては,コスト的に,イオン液体以外の系の開発が課題となるようには思われる。)
----------------------容量の算出法についての検証---------------------------
(電気化学測定)Pyrolytic graphite (PG) foil 熱分解黒鉛箔,Pyrolytic graphite (PG) foil 熱分解黒鉛箔 系
A Swagelok-type cell (1/2 inch diameter) was constructed using a ~4 mg PG foil (0.017 mm, Suzhou Dasen Electronics Materials) cathode and a 90 mg Al foil (0.25 mm, Alfa Aesar) anode.
電気化学測定用のセルは,Swagelok 型セル(直径 1 / 2 インチ)に,
~ 4 mg PG 箔 ( 0.017 mm 、 Suzhou Dasen Electronics Materials) のカソ ー ドと
90 mg の AI 箔 ( 0.25 mm 、 AIfa Aesar) のアノ ー ド
をセットすることで作成している。
↑
カソードとして用いられているPG箔( 熱分解黒鉛箔)の重量に対してアルミ箔の重量が大過剰であるので,
電池容量(mAh/g)は,カソードに用いたカーボン材料の重さあたりで算出している。
1ページ目右カラム20行目,
The optimal ratio of AlCl3/[EMIm]Cl was found to be ,1.3–1.5 (Extended Data Fig. 2a),
affording a specific discharging capacity of
60–66 mAh/g (based on graphitic cathode mass) with a Coulombic efficiency of 95–98%.
↑
グラファイトカーソードの重量基準で60~66 mAh/gとされている。
電池容量の算出に関しては,論文本文では具体的な記述がなかなか読み取れなかったが,
論文に付属のSI (Supporting Information) で見ることができる。
”Extended Data Figure 3 | Calculated discharging capacities of Al/graphite cells with different masses of graphitic materials.”
では,Graphitic material mass (mg)とCapacity (mAh) を複数サンプルに対してプロットして,その直線性とスロープを表示しており,
電池容量(mAh/g)は,カソードに用いたカーボン材料重さあたりで算出していることがわかる。
Extended Data Figure 3aは,
天然黒鉛箔におけるカーボン材料の重さ(mg)と容量(mAh)のプロットになっており,
そのスロープ(mAh/mg)は,
天然黒鉛箔(厚さ 50μm):0.05697(mAh/mg) → 容量 56.97 (mAh/g) (mg→gで1000倍)
天然黒鉛箔(厚さ 130μm):0.05853(mAh/mg) → 容量 58.53 (mAh/g)
Extended Data Figure 3bは,
熱分解黒鉛(PG)箔とグラファイトフォームにおけるカーボン材料の重さ(mg)と容量(mAh)のプロットになっており,
そのスロープ(mAh/mg)は,
熱分解黒鉛(PG)箔: 0.04545(mAh/mg)→ 容量 45.45 (mAh/g) (mg→gで1000倍)
グラファイトフォーム: 0.05146(mAh/mg)→ 容量 51.46 (mAh/g) (mg→gで1000倍)
↑
Extended Data Figure 3からは,以上のように単純計算されるのだが,
これらの値は,著者らが論文本文で述べている,
”specific discharging capacity of 60–66 mAh/g (based on graphitic cathode mass) "
の記述とは一致していない。
以下では,容量の電流密度依存性について検証するが,多価金属二次電池の場合特に,
電池容量は電流密度(あるいは電解質組成)等の実験条件に非常に敏感であり,
本文中で容量を算出した実験条件と,Extended Data Figure 3での実験条件とが異なっていることも考えられるが,
それを知ることのできるパラメータが明確となっていない。
ところで,グラファイトフォーム(スポンジ状の多孔質構造を有するグラファイト)のSEM像がFig.2aに示されており,
約300μmの空隙からなる多孔質構造となっている。その構造からは,容量の増加が期待されるのだが,
天然黒鉛箔よりも容量低下してしまっている。
その原因としては,カーボン材料の抵抗率が多孔性のグラファイトフォームでは増加してしまって,
セルの内部抵抗が上がってしまっていることも考えられるのかもしれない。
-----------------容量の電流密度依存性: PC(熱分解黒鉛箔)の場合 ------------------
The Al/PG cell was then charged (to 2.45 V) and discharged (to 0.01 V) at a current density of 66 mA g–1 with a MTI battery analyser (BST8-WA) to identify the ideal AlCl3/[EMIm]Cl mole ratio (Extended Data Fig. 2a).
To investigate the Coulombic efficiency of the Al/PG cell in AlCl3/[EMIm]Cl < 1.3 (by mole) electrolyte, the cell was charged to 2.45, 2.50, 2.55 and 2.60V, respectively, and discharged to 0.4 V at a current density of 66 mA g–1 (Extended Data Fig. 6a).
電解電解質 AlCl3/[EMIm]Clの最適比を求める際には,66 mA/g の電流密度で,
充電側のカットオフ電圧を2.45V,
放電側のカットオフ電圧を0.01V
として測定している。
クーロン効率(充電された電気量に対し放電された容量の比)を求める際には,66 mA/g の電流密度で,
充電側のカットオフ電圧を2.45, 2.5, 2.55, 2.60V,
放電側のカットオフ電圧を0.4V
として測定している。
ここで,電流密度66 mA/gに関しては,2ページ左カラム9行目で,
66 mA/g (1 C charging rate)
されている。
C(Capacity)レートとは,バッテリー容量(Ah)に対する充電(放電)電流値(A)の比であり,
定電流充放電測定の場合、電池の容量を1時間で完全充電(または放電)させる電流の大きさを1Cと定義されている。
これにより、容量の異なる(電極活物質の重量や体積の異なる)電池同士の特性・条件をそろえて比較するすることができる。
この論文の実験では,カソードに用いたカーボン材料の重さを基準として電池容量(mAh/g)が算出されているので,
カソードを4 mg PG 箔(重量が減ればそれに比例して電流値も減少)
とした場合の実験条件としては,
充電(放電)時間を1hとした場合,
66 (mA/g) x 0.004 (g) = 0.264 mA (264μA)定電流での充放電特性の測定になる。
実験に用いたPG箔の面積がわからないが,Swagelok 型セル(直径 1 / 2 インチ)から,直径1/2インチ(1.27cm)として計算すると,
単位面積(cm2)当たりの電流密度で表せば,
0.264mA/ 1.27(cm2) = 0.209 mA/cm2
約0.2 mA/cm2 となる。
以上は,充電(放電)時間を1時間とした場合の電流密度設定であり,
充電(放電)時間が変われば電流密度の設定時間も変わってくる。
Fig.1の挿入図で,充放電曲線が示されており,10時間で,充放電が5サイクルとなっており,
それが換算された時間になっていなければ,充電および放電は,各1時間と考えられる。
↑電流密度を,マグネシウム金属等の多価金属イオン電池とで比較しようとした場合,
多価金属イオン電池では,ほとんどの場合,電流密度は,単位面積当たり(mA/cm2)で表記されており,
0.2 mA/cm2前後が,電流密度を上げていって容量減少が起こりだす臨界域となっている場合が多いと思う。
この論文では,電流密度がmA/g 表記であるので比較が難しいのだが,上記のような変換を当てはめて比較を行ってみる。
”Extended Data Figure 7 | Rate capability of an Al/PG cell”,PC(熱分解黒鉛箔)の場合に関して,
電流密度(mA/g )を変化させたときの容量(mAh/g)変化のグラフが示されている。
その値を,放電に関して,グラフから概略読みとって書き出すと,
電流密度 66 mA/g (約0.2 mA/cm2) → 容量 約63 (mAh/g)
電流密度 99 mA/g (約0.3 mA/cm2) → 容量 約60 (mAh/g)
電流密度 132 mA/g (約0.4 mA/cm2) → 容量 約55 (mAh/g)
電流密度 165 mA/g (約0.5 mA/cm2) → 容量 約43 (mAh/g)
電流密度 264mA/g (約0.8 mA/cm2) → 容量 約25 (mAh/g)
↑
論文で記述のないパラメータがあるために,正確な検証はできないのだが,
やはり,電流密度の増加とともに,容量は減少しており,
1 (mA/cm2)以上の電流密度での充放電は,Pyrolytic graphite (PG) 箔をカソードとした場合には難しいように考えられる。
これらの特性に関しては,この時点では,マグネシウム二次電池系との比較で,大きな違いはないように思われる。
----------------------- 容量の電流密度依存性:グラファイトフォームの場合---------------------------------------
PC(熱分解黒鉛箔)の場合は,顕著な電流密度依存性が観測されたのに対して,
グラファイトフォームの場合には,電流密度の影響が劇的に少なくなることが報告されている。
これは,以下のFig.2aで示されている。
(Extended Data Figure 9 のほうが,電流密度依存性を議論するために最適なデータには思われる。)
Remarkably, the Al/graphitic-foam cell (in a pouch cell configuration) could be charged and discharged at a current density up to 5,000 mA /g, about 75 times higher (that is, at a 75 C rate, ,1 min charge/discharge time) than the Al/PG cell while maintaining a similar voltage profile and discharge capacity (~60 mA h/ g ) (Figs 1b and 2b).
↓
注目すべきことに、 A l/グラファイト発泡セル(ラミネート型のパウチセル構成)は、
同様な電圧プロファイルと放電容量(約 60 mAh/g )を維持しつつ,
Al/PG(熱分解グラファイト)よりも約 75 倍高い最大 5000 mA /g の電流密度での充電および放電が可能あった
(つまり、 75Cのレ ー ト,1 分間での充放電)(Fig.lb および 2b )。
An impressive cycling stability with ,100% capacity retention was observed over 7,500 cycles with a Coulombic efficiency of 97 +-2.3% (Fig. 2c).
↓
容量保持率 100% の優れたサイクル安定性が 7,500 サイクルにわたって観察され、クーロン効率は 97±2.3% だった (Fig.2c)。
This is the first time an ultrafast Al-ion battery has been constructed with stability over thousands of cycles.
The Al/graphitic-foam cell retained similar capacity and excellent cycling stability over a range of charge– discharge rates (1,000–6,000 mA/g) with 85-99% Coulombic efficiency (Extended Data Fig. 9a).
↓
数千サイクルにわたって安定性を備えた,超高速アルミニウムイオン電池が初めて構築された。
Al/グラファイト発泡セルは、85-99%のクーロン効率で、充放電速度(1,000~6,000 mA/g)にわたって,同様な容量と優れたサイクル安定性を維持した(拡張データ図9a)。
Fig.2cとExtended Data Fig. 9aとを比較すると,それらの特性に合致しない点があるのだが,実験条件がやや異なっているのかもしれない。しかし,実験条件やパラメータが,すべては記載されてはいないため,議論が難しい点がある。
例えば,以下のFig.2で,電流密度5000mA/gnと100mA/gとの場合を比較すると,電流密度の高い5000mA/gの場合のほうがやや高い容量(mAh/g)を示しているのに対して,
Extended Data Fig. 9aのデータでは,電流密度5000mA/gnと1000mA/gとの場合が比較できて(Fig. 9bには100mA/gのデータがあるのに,Fig9aには無し),電流密度の高い5000mA/gの場合よりも,電流密度の低い100mA/gの場合ほうが高い容量(mAh/g)を示している。
Al/グラファイトフォームが,二次電池である場合には,その充放電反応は酸化還元の化学反応に基づいているので,後者の結果のほうがリーズナブルだと考えられる。
Extended Data Fig. 9bには,実際の充放電曲線が示されているのだが,
100 mA/gで, 約34分で放電がカットオフとなっており,
そうすると,5000mA/gの場合の放電カットオフまでの時間は,約41秒となる。
これだけの急速充放電は,充放電反応が酸化還元の化学反応に基づいている二次電池では,困難ではないだろうか?
スーパーキャパシタ(電気二重層キャパシタ)的な挙動に近いようにも思われる。
多価金属イオン二次電池では,金属極でのイオン化や還元の速度がネックとなって,電流密度を上げることが困難となっているという課題がある。
-----------------------論文成果のハイライト-----------------------------------------
上記のような,Al/グラファイトフォーム(発泡体)セルの特性から,著者らは以下のように述べている。
■The cathode was found to enable fast anion diffusion and intercalation, affording charging times of around one minute with a current density of 4,000 mA/g (equivalent to 3,000 W /kg).
このカソード(グラファイト発泡体カソード)は,アニオンの高速拡散とインターカレーションを可能にし、電流密度 4,000 mA/g (3,000 W/kg のパワー密度に相当) で約 1 分間で充電できることがわかった。
(電池容量的には,60mAh/g前後であるので,これまでの他の多価金属イオン二次電池に比べて同等か,場合によっては低いものとなっているが,高電流密度下での高速充放電特性(高パワー密度)が,この論文の成果のハイライトになっている。)
---------------------------------------------------------------------------------------------------
(↓論文内容の理解・議論に図表の表示が不可欠のため,著者らによってResearch GateにアップロードされているFig.2のURLに直接アクセスすることで,直接リンクでFig.2を以下に表示させていただいております。著作権上問題がある場合にはご指摘ください。削除いたします。)

Fig.2 An ultrafast and stable rechargeable Al/graphite cell. a, A scanning electron microscopy image showing a graphitic foam with an open frame structure; scale bar, 300 μm. Inset, photograph of graphitic foam; scale bar, 1 cm. b, Galvanostatic charge and discharge curves of an Al/graphitic-foam pouch cell at a current density of 4,000 mA g−1. c, Long-term stability test of an Al/graphitic-foam pouch cell over 7,500 charging and discharging cycles at a current density of 4,000 mA g−1. d, An Al/graphitic-foam pouch cell charging at 5,000 mA g−1 and discharging at current densities ranging from 100 to 5,000 mA g−1.
----------------------- Al/グラファイトフォームセルの構造と実験条件の確認 ---------------------------------------
METHODS
・・・・・
Pouch cells were assembled in the glove box using a graphitic-foam (~3 mg) cathode and an Al foil (~70 mg) anode, which were separated by two layers of glass fibre filter paper to prevent shorting. Polymer (0.1 mmx4 mmx5 mm) coated Ni foils (0.09 mmx3 mmx60 mm in size; MTI corporation) were used as current collectors for both anode and cathode. The electrolyte (~2 ml prepared using AlCl3/[EMIm]Cl = 1.3 by mole) was injected and the cell was closed using a heat sealer.
↓
パウチセル(ラミネート型)は、グラファイトフォーム(~3 mg)カソードとAlフォイル(~70 mg)アノードを用いてグローブボックス内で組み立てられ,短絡を防ぐために2層のガラス繊維濾紙で分離された。 ポリマー(0.1mmx4mmx5mm)で被覆されたNi箔(サイズ0.09mmx3mmx60mm、MTI社)を、アノードおよびカソードの両方の集電体として使用した。 電解液(~2 ml,AlCl3/[EMIm]Cl = 1.3 モル比で調製)を注入し、ヒートシーラーを使用してセルを密閉した。
上記から,
グラファイト発泡体:~3 mg
Al箔:~70 mg
であるので,この場合もアノード側のアルミニウム過剰の条件として,
容量,エネルギー密度,パワー密度等の算出は,カソード側の グラファイト発泡体の重量基準となっていると思われる。
ラミネート型のパウチセルで実験が行われているが,
カソードであるグラファイトフォーム,アノードであるAl箔の面積の記述がないので,
とりあえず,集電体幅での面積(3mmx50mm,1.5cm2)で考えることとする。
電流密度 100(mA/g)→ 0.3 mA → 面積当たりの電流密度 0.20 (mA/cm2)
電流密度 500(mA/g)→ 1.5 mA → 面積当たりの電流密度 1.00 (mA/cm2)
電流密度1000(mA/g)→ 3.0 mA → 面積当たりの電流密度 2.00 (mA/cm2)
電流密度4000(mA/g)→ 12 mA → 面積当たりの電流密度 8.00 (mA/cm2)→パワー密度:3,000 W /kg
電流密度5000(mA/g)→ 15 mA → 面積当たりの電流密度 10.00(mA/cm2)
電流密度4000(mA/g)は確かにかなり高い値となっているが,
~1000(mA/g)前後であれば,他の多価金属イオン二次電池においても視界に入るレベルのように思われる。
------------------------充放電反応機構------------------------------------------------
著者らは以下のように述べている
where n is the molar ratio of carbon atoms to intercalated anions in the graphite. The balanced AlCl4– and Al2Cl7– concentrations in the electrolyte allowed for an optimal charging capacity at the cathode, with abundant AlCl4– for charging/intercalation in graphite (equation (2)), and sufficient Al2Cl7– concentration for charging/electrodeposition at the anode (equation (1)).
↓
ここで,n は,グラファイト中での,炭素原子と挿入アニオンのモル比である。
電解質中のバランスの取れた AlCl4- および Al2Cl7- 濃度により、カソードでの最適な充電容量が可能になり、
AlCl4のグラファイト中への充電(インターカレーション,式 (2))と,
アノードでの充電(電着)に十分な Al2Cl7- 濃度が得られる (式(1))。
著者は,
カソードでは,グラファイト中へのAlCl4- のインタカーレーション(充電)・デインターカレーション(放電)が起こり,
アノードのAl極では,上記(1)式で表されるアルミニウムの酸化還元反応が起こる,
と説明している。
アノード側では,
充電では,Al2Cl7- がアルミニウム電極表面に電着して析出し,
放電では,アルミニウムがイオン化して,電解質中のAlCl4-と反応し,イオン種Al2Cl7- が形成される。
式(1)の可逆な化学反応が,物理吸着機構によって充放電を行うスーパーキャパシタの充放電並みの速度で起こっている,
ということになる。
(Al電極側は通常の素のAl箔であるので,そのようなAl電極表面で上記のようなことが起こり得るのか,と問われれば,
これまでの経験からは,それは難しいと答えざるをえないように思う。
そこに,新しい科学があるのかもしれないが。)
■The present Al/graphitebattery can afford an energy density of ,40 W h/kg (comparable to lead–acid and Ni–MH batteries, with room for improvement by optimizing the graphitic electrodes and by developing other novel cathode materials) and a high power density, up to 3,000 W/ kg (similar to supercapacitors). We note that the energy/power densities were calculated on the basis of the measured ,65 mAh/g cathode capacity and the mass of active materials in electrodes and electrolyte.
↓
Al/グラファイトバッテリーは、40 W h/kgのエネルギー密度(鉛蓄電池やニッケル水素バッテリーに匹敵するが、黒鉛電極の最適化や他の新しい正極材料の開発による改善の余地がある)を実現でき、パワー密度、最大 3,000W/kg (スーパーキャパシタと同様)。
エネルギー/出力密度は、測定された 65 mAh/g のカソード容量と、電極および電解質内の活物質の質量に基づいて計算されたことに注意されたい。
↑
アノードのアルミニウムは過剰としているので,カソードとしたグラファイトフォーム(発泡体)の重量基準となっていると思われる。
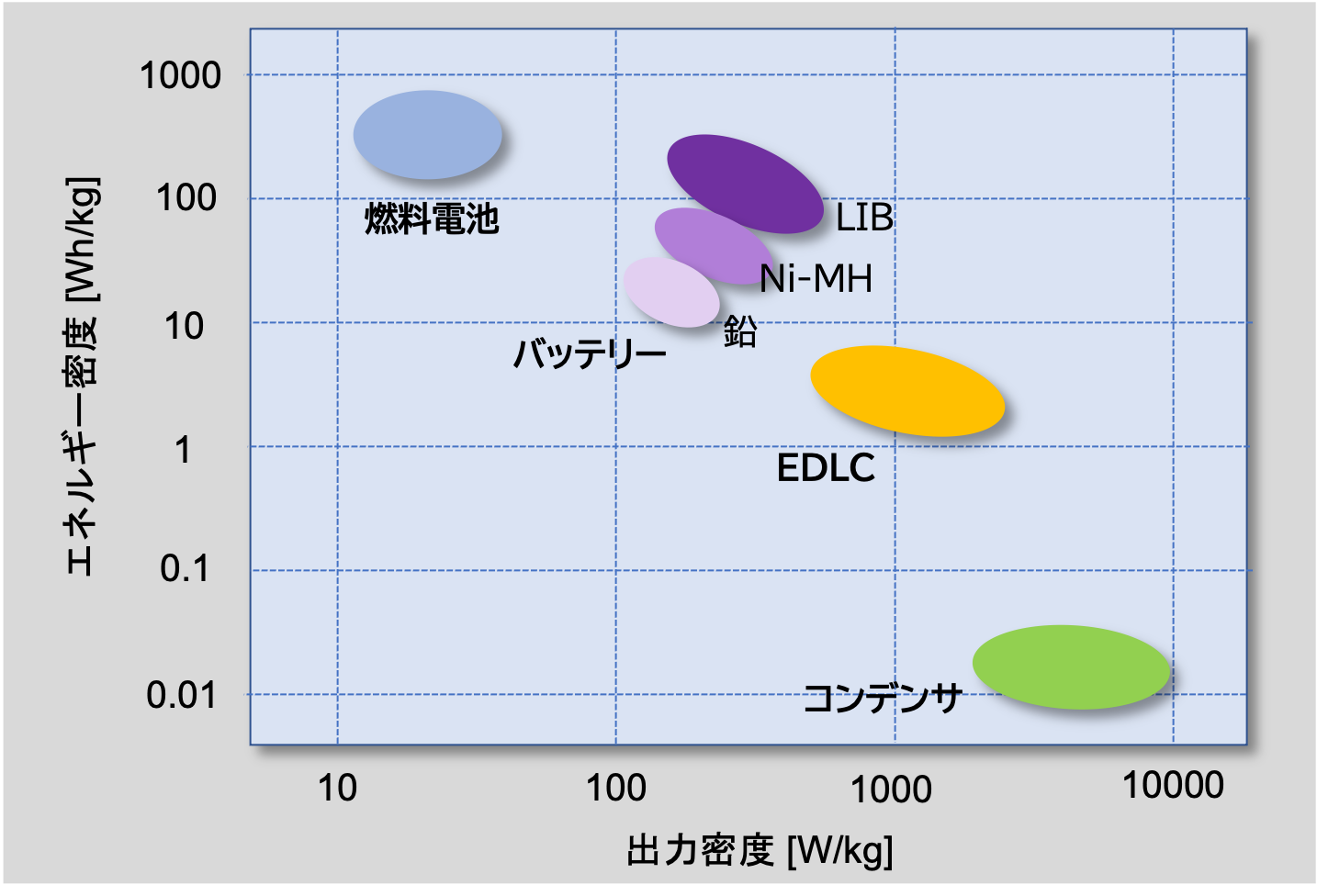
以下のRagonプロットで,
エネルギー密度:40 W h/kg
パワー密度:3,000 W/ kg
の位置を確認してみるとわかるように,
パワー密度3000W/kgであるので(実験的にはExtended Data Figure 9 で,さらにその1.5倍のパワー密度となっている),
スーパーキャパシタというよりは,アルミ電解コンデンサー等のコンデンサーに近い値となっている。
(↓論文内容の理解・議論に以下の図の表示が不可欠のため,直接リンクでダイレクトに表示させていただいております。
著作権上問題がある場合にはご指摘ください。削除いたします。)
(出典:エーアイシーテック株式会社ホームページ,電気二重層キャパシタの基礎知識)
https://www.aictech-inc.com/information/capacitor_foundation02.html
https://www.aictech-inc.com/information/images/c02/c02-001.png
-------------------------------------おわりに---------------------------------------------
多価金属二次電池の可能性を大きく広げた点,目標となる点(マイルストーン)を一挙に遠い地点まで持っていった点で,
画期的な成果の論文になっていると思われる。
ただし,Al/グラファイトフォームセルが,従来の多価金属イオン電池に分類されるかどうかに関しては,
検討すべき課題が多いように思われる。
カソード材料となる熱分解黒鉛(PG)箔とグラファイト発泡体とで,非常に大きなパワー密度の違いが現れているが,
これはグラファイト発泡体の多孔質性に加えて,両者への電解質の濡れ性の違いが影響しているようにも思われる。
イオン液体をいじった経験では,イオン液体は種々の材料表面との親和性が高くはなく,濡れ性が悪かったような記憶がある。
このため,熱分解黒鉛(PG)箔では,イオン液体電解質が,PGの細孔に十分に充填されないのではないだろうか。
GMG社のグラフェンーアルミニウムイオンバッテリーでは,この点が改良されて,
さらに容量およびパワー密度が向上しているのかもしれない。
引き続き,GMG社グラフェンーアルミニウムイオンバッテリーまわりの,一次資料の検索と検証を続けていく予定です。
