多価金属二次電池,アルミニウム二次電池,マグネシウム二次電池,全固体型マグネシウム二次電池,全固体マグネシウム二次電池,マグネシウムヨウ素iイオン二次電池,マグネシウムヨウ素二次電池、積層型電解質,マグネシウム二次電池固体電解質,スーパーキャパシタ,電気二重層キャパシタ,Rechargeable magnesium battery,
非液体電解質,高分子ゲル電解質,IRドロップ,フレキシブル
全固体 多価金属二次電池に向けて No2.
固体電解質
2023.8.21
固体電解質
私たちは,これまでに平面型マイクロスーパーキャパシタ(micro-super-capacitor, MSC, 電気二重層キャパシタ)の研究開発を行ってきており,その特性の改良を進める過程で,非液体電解質型のマグネシウム二次電池の可能性の一つに行き着いています。
平面型MSCは,カーボンくし形電極と高分子ゲル電解質とからなるフレキシブルで薄型のエナジーストレージデバイスです。高分子ゲル電解質としては,例えば,ポリビニルアルコール(PVA)水溶液に酸や無機・有機金属塩を添加し乾燥することでゲル化したものが用いられます。論文発表等でチャンピオンデータを得るためには,拡散性の高い原子サイズの小さなプロトン(H+)の吸脱着が起こる硫酸(H2SO4)系が多く用いられます。しかし,ウェアラブル用途を考えた場合には,硫酸等の強酸を用いることは避けなければなりません。使用できるとすれば,無機・有機金属塩が考えられますが,問題はそれらのPVA膜への溶解性と電気化学的な特性となります。
アルカリ金属ハロゲン塩を考えた場合,アルカリ金属イオンとしては,Li+,Na+,K+となります。原子半径のみを考えた場合には,サイズはLi+ < Na+ <K+ となり,リチウム塩が好ましいと思われますが,アルカリ金属イオンは溶媒和分子を周りにまとった形で振舞いますので,溶媒和半径で考えると,サイズは,Li+ > Na+> K+ となります。実際,MSCの静電容量の大きさは,ハロゲン原子が同じ場合,溶媒和半径が小さいほど静電容量が高く,Li塩 < Na塩 < K塩の順となります。
高分子ゲルへの溶解性に関してですが,ハロゲン化金属塩の場合には,イオン結合性の高い塩ほど溶解性が高くなり
ます。ハロゲン化カリウムの水溶液での溶解性(20℃付近)で見ますと,KCl (34g/水100g),KBr (65g/水100g),KBr (148g/水100g)となります。ヨウ化カリウムは,極めて溶解性が高く,また,水溶液を塗布して乾燥することで得られるゲル化PVA膜に,より高濃度で,析出することなく添加できます。塩素系や臭素系のハロゲン化金属塩の場合には,ゲル化したPVA膜の乾燥ですぐに白色の塩が析出した状態となり,電気化学的な特性も同時に劣化します。ヨウ化カリウム(KI)を,析出を抑えてさらに高濃度でPVA膜中に添加するためには,多価のアルコール類の添加が有効です。これは,ヨウ化カリウムが多価アルコールに良好な溶解性を示すためです。これによって,PVA水溶液,PVA架橋剤,ヨウ化カリウム,多価アルコール等の混合水溶液を塗布して乾燥して得た膜において,水がほぼ除かれた状態となっても(一部の水はカリウムイオンの水和構造として残る),ヨウ化カリウムの析出を無くすることができます。そのような状態の膜は,ゲル膜というよりは,固体高分子膜に近い状態となっています。多価アルコールは,固体高分子膜に柔軟性を付与するための可塑剤としても働いています。このため,上記のような非液体電解質は,固体電解質とみなせる状態のものとなっています。
上記のような電解質は,有機溶媒を必要としない簡便な水系プロセスでの製造が可能ですので,調製プロセスにおける水や酸素の影響をほとんど受けません。これは,厳密に水や酸素の影響を除いた製造プロセスが必要となるリチウムイオン電池に比べて,有利な点となります。これによって,電池製造のプロセスコストを大幅に低減することができます。
以上のような経緯で,ヨウ化カリウムを含む電解質膜を使うスーパーキャパシタの検討を行うようになったために,必然的にマグネシウム二次電池の分野に近づくことになりました。
電気化学的特性
上記のヨウ化カリウムを含む固体電解質の電気化学的な特性を,サイクリックボルタンメトリー測定からFig.1に示しました。Fig.1は,ヨウ化カリウム/PVA電解質からなる平面型MSC(多孔質カーボン電極)のサイクリックボルタモグラム(掃引速度10mV/s)です。容量性電流に加えて,何らかの酸化還元波が現れています。Fig.2には比較として,リチウムイオン電池系で使われることのある有機金属塩のLiTFSI(リチウムビス(トリフルオロメタン)スルホンイミド)/PVA電解質系でのサイクリックボルタモグラムを示しましたが,容量性電流からなるキャパシターに特徴的な,酸化還元波のピークのない形状となっています。両者を静電容量で比較しますと,前者(Fig.1)が4.6 mF/cm2,後者が8.7mF/cm2となり,ヨウ化カリウム系のほうが大きくなっています。このように,容量電流に加えて酸化還元電流を伴うような系は,疑似スーパーキャパシタと呼ばれ,そのようなMSCの静電容量は,酸化還元波の電流の重なりによって大きくなります。
この時の酸化還元反応には,ヨウ素イオンが関わっていることが当然予想されます。電極反応 I2 + 2e- ⇔ 2I- の酸化還元電位は0.54Vです。MSCセルの場合には,参照極が設けられていいませんので正確な議論はできませんが,Fig.1のサイクリックボルタモグラムにおいては,0.8V付近に酸化反応のピーク,0.35V付近に還元反応のピークが現れています。これをMSCの定電流モードでの充放電曲線で測定すると,Fig.3のような結果となります。充電時の0.8V付近の酸化反応および放電時の0.35V付近の還元反応に起因する電圧が明確に示されています。疑似スーパーキャパシタの場合には,このようなヨウ素の酸化還元反応は,静電容量増加のための因子として働きます。しかし,放電電位が急激にドロップしてしまう特性(電池のIRドロップ的な特性)等は,スーパーキャパシタの特性として好ましいものではありません。そこで,放電電位の低下を解決することを目的として,非対称な電極構造のMSCの検討を行いました。片側の電極を,Cu(酸化還元電位0.34V), Zn(酸化還元電位-0.76V), Mg(酸化還元電位-2.36V)に代え,実験上の制約から(レーザー加工できる厚さの金属板の入手が困難であったことから),セルの構造は,くし形電極からなる平面型MSCではなく,従来のサンドイッチ構造のMSCとしました。結局,それらの構造は電池そのものでした。
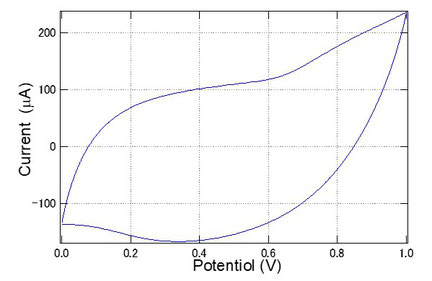
Fig.1 ヨウ化カリウム/PVA電解質からなる平面型MSC(多孔質カーボン電極)のサイクリックボルタモグラム(掃引速度10mV/s).

Fig.2 LiTFSI/PVA電解質系からなる平面型MSC(多孔質カーボン電極)のサイクリックボルタモグラム.

Fig.3 ヨウ化カリウム/PVA電解質からなる平面型MSC(多孔質カーボン電極)の充放電曲線.
私たちが検討を進めている全固体型マグネシウム二次電池では,負極となるマグネシウムとヨウ素イオンとの間での酸化還元反応がベースとなっています。このとき,正極側では上記のようなヨウ素イオンの関与する酸化還元反応が起こり得ます。それは,マグネシウム二次電池の特性において,決して好ましいものではありませんでした。そのため,私たちは,積層型電解質マグネシウム二次電池において,複数の層構造によって,正極側と負極側での電気化学反応に係わる化学種を規制し,それによって,IRドロップ(IR損)につながる現象の抑制を可能としました。現在,このようなマグネシウム二次電池の特性をさらに向上させるための研究開発を進めています。
